无锡奥克丹生物科技有限公司官方网站欢迎您!

0510-85214012
03产品咨询Product consultation
发布时间:2025/06/13文章来源:无锡奥克丹生物科技有限公司
一、为什么氨氮检测如此重要?
氨氮(NH₃/NH₄⁺)是水体中常见的污染物,主要来源于工业废水、农业径流和养殖饲料残留。其危害包括:
环境水:过量氨氮导致水体富营养化,破坏生态平衡;
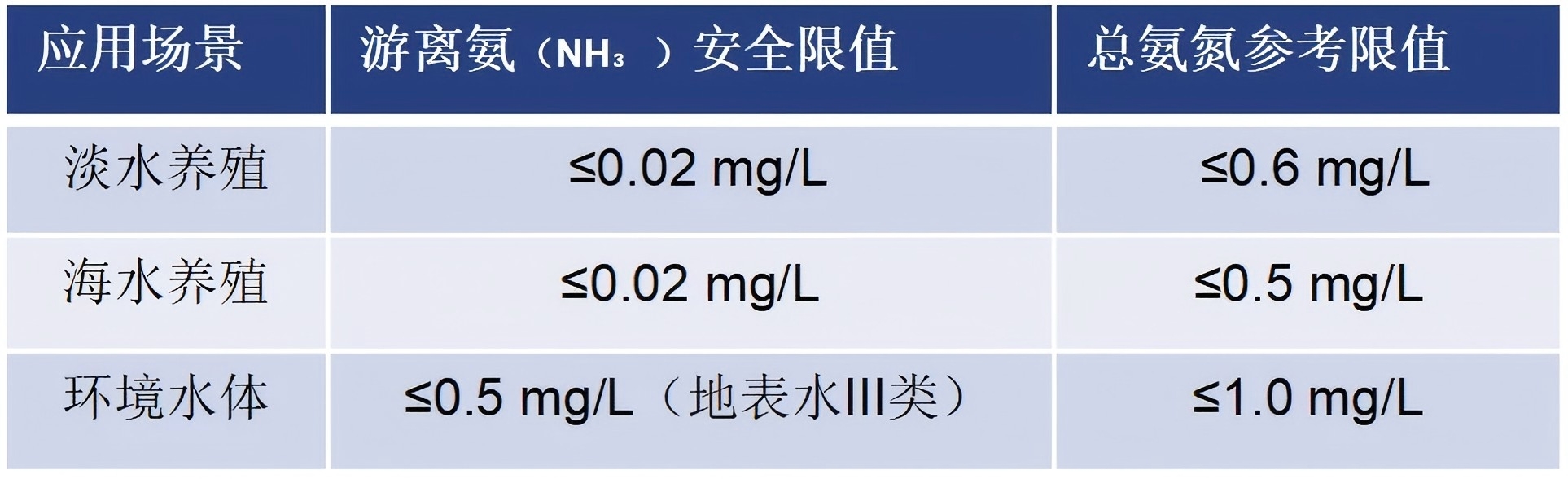
养殖水:游离氨(NH₃)毒性强,0.02mg/L即可引发鱼类急性中毒,造成大规模死亡。
不同场景的安全标准:
二、核心技术:纳氏试剂分光光度法
我们的便携式分析仪采用纳氏试剂法,结合分光光度技术,实现快速、精准的氨氮检测:
1.检测原理
化学反应:水样中的氨氮与纳氏试剂(碘化钾、碘化汞的强碱溶液)反应,生成淡红棕色络合物(NH₂Hg₂OI)。
吸光度测定:特定波长(420 nm)下,络合物的吸光度与氨氮浓度成正比,仪器通过光信号转换计算浓度值。

2.水产养殖业涉及到的氨氮计算方法
使用便携式水质分析仪检测氨氮时,仪器通常直接显示的是 “氨氮(NH₃-N)浓度”,即以氮(N)为计量单位的氨氮含量(单位:mg/L)。如果需要将这一数据转换为铵离子(NH₄⁺)的浓度,需通过简单的化学计量换算。以下是具体步骤和示例:
1.铵离子(NH₄⁺)
铵离子(NH₄⁺)的分子量计算:
14(N)+ 4×1(H) = 18
换算公式:
NH₄⁺ 浓度 = NH₃-N 浓度 ❌ 18 ➗ 14
NH₄⁺ 浓度 ≈ NH₃-N 浓度 ❌ 1.286
假设仪器测得水样中氨氮(NH₃-N)浓度为1.0 mg/L;
换算为 NH₄⁺ 浓度:
1.0 mg/L×1.286=1.286 mg/L(以 NH₄⁺ 计)
1.氨分子(NH3)
氨分子(NH₃)是水产养殖和水体环境中最具毒性的污染物之一,其危害远超离子态铵(NH₄⁺)。
氨分子的毒性随环境参数动态变化,需重点关注:
pH值
pH每升高1单位,游离氨(NH₃)占比增加约10倍。
例如:
pH=7.0时,NH₃仅占0.6%;
pH=8.5时,NH₃占比飙升至15%~20%。
水温
水温从20℃升至30℃,NH₃占比翻倍(因解离常数Kₐ随温度升高而增大)。
换算公式:
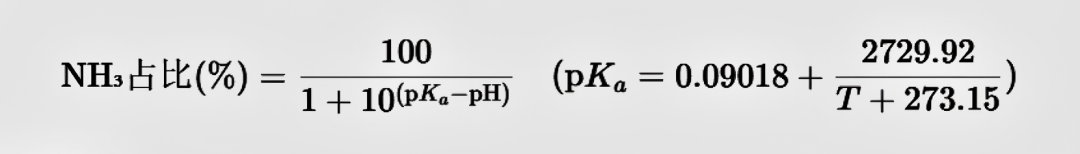
(T为水温,单位℃)
奥克丹便携式水质分析仪内置氨氮换算计算器,是针对水产养殖场景植入的智能化功能模块,实现总氨氮(NH₃-N)与毒性更强的非离子氨(NH₃)浓度的实时换算。
如下图所示:




三、总结
常规管理:直接使用仪器显示的 NH₃-N 浓度(mg/L)判断水质是否安全。
特殊需求:按需通过系数 1.286(NH₄⁺) 转换。
毒性评估:若需分析游离 NH₃ 的毒性,需结合水温、pH 值进一步计算(可通过仪器内置功能辅助计算获得)。
通过以上步骤,养殖户可快速将检测数据转换为所需的浓度形式,科学管理水质,确保养殖安全。